碳酸钠,俗称纯碱或苏打,是日常生活中一种极为重要的基础化学品。它不仅是制造玻璃、肥皂、纸张等工业产品的关键原料,也作为软水剂、清洁剂广泛应用于家庭场景。在化学实验室中,我们可以通过模拟工业“氨碱法”(索尔维法)的原理,利用氯化钠(食盐)、二氧化碳和氨气为原料,通过一套精心设计的装置来制备纯碱,从而深入理解这一日用化学品背后的制造科学。
一、 实验原理与核心反应
本制备方法基于著名的“氨碱法”,其核心在于利用氨气提高二氧化碳在饱和食盐水中的溶解度,并促使碳酸氢钠沉淀析出,再经加热分解得到碳酸钠。主要分两步进行:
1. 碳化与沉淀:向饱和食盐水中通入足量的氨气,形成氨盐水。随后通入二氧化碳,发生如下反应,生成溶解度较小的碳酸氢钠(小苏打)晶体:
NH₃ + CO₂ + H₂O + NaCl → NaHCO₃↓ + NH₄Cl
2. 分解制纯碱:过滤得到碳酸氢钠固体,经洗涤后加热煅烧,分解生成最终产品碳酸钠:
2NaHCO₃ → Na₂CO₃ + CO₂↑ + H₂O↑
二、 实验装置与关键步骤
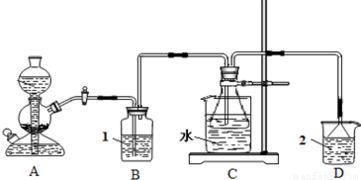
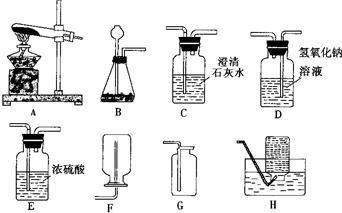
典型的实验室装置通常包括气体发生、净化、反应及尾气处理等部分。
- 装置气密性检查:实验开始前,必须首先检查整个装置的气密性,这是确保反应物有效利用和安全操作的前提。通常采用微热或液封法检查连接处是否漏气。
- 试剂加入与氨化:向反应容器(如锥形瓶)中加入饱和食盐水,然后通入氨气(可由浓氨水加热或铵盐与碱反应制得),制成氨盐水。
- 二氧化碳的通入与碳化:将二氧化碳气体(可由大理石与稀盐酸反应制得,经饱和碳酸氢钠溶液净化)通入氨盐水中。此时可观察到溶液逐渐变浑浊,有大量白色细晶(NaHCO₃)沉淀生成。需控制通入速度,保证充分反应。
- 产品的分离与转化:反应结束后,通过过滤分离出碳酸氢钠固体,用少量冷水洗涤以去除附着杂质。将洗净的固体置于蒸发皿中,用酒精灯或马弗炉小心加热至不再有气体和水汽产生,即得到白色的碳酸钠粉末。
三、 联系工业生产与日用意义
这套实验室模拟装置,本质上是庞大化工生产体系的微型缩影。大规模的纯碱生产同样遵循此化学原理,但在设备规模、热量回收、原料循环(如回收氨气)和副产品(如氯化钙)处理上更为复杂高效。
正是通过这样的化学过程,廉价的食盐(氯化钠)得以转化为用途广泛的纯碱。它随后进入千家万户和各行各业:调节面食的pH、作为洗衣粉的助洗剂、处理生活用水……其制备过程本身,就是化学将天然资源转化为服务人类生活的产品的生动例证。通过动手实验,我们不仅掌握了制备一种具体化学品的方法,更深刻体会到日用化学产品制造如何将基础科学原理与日常生活需求紧密相连。